Willkommen in der Praxis Dr Bull
Ihr Spezialist für Endoskopie, Proktologie und Venenchirurgie
Sehr geehrte Damen und Herren!
Dr. Bull ist Facharzt für Chirurgie in Wien und praktiziert seit 1994 ausschließlich ambulant durchzuführende Eingriffe. Die Ordination ist spezialisiert auf Endoskopie (Gastro- und Koloskopie), Proktologie und Venenchirurgie. Die Chirurgische Tagesklinik Sievering und die im Zentrum der Stadt befindliche Privatpraxis im Heiligenkreuzerhof liegen im Trend der heutigen Entwicklung: die vorsorgliche endoskopische Untersuchungen und viele Operationen erfordern heute keinen Krankenhausaufenthalt mehr: sie können in einem ambulanten chirurgischen Zentrum bzw. einer Tagesklinik vorgenommen werden. Medizinische Versorgung, Betreuung sowie chirurgische Ausstattung entsprechen dem höchsten Niveau; dazu umgibt Sie eine private Atmosphäre.
Auf unseren Internetseiten finden Sie zusätzlich zur Ordination und chirurgischen Praxis, wichtige Patienteninformationen, entweder in Form von Krankheitsbildern oder in alphabetischer Auflistung. Bei Fragen können Sie sich jederzeit an ihren Venenarzt in Wien wenden.

Dr Bull
Tageschirurgie
Ambulantes Operieren: Unter Tageschirurgie oder auch Ambulantoperation versteht man die Durchführung eines operativen Eingriffs ohne anschließenden mehrtägigen Spitalsaufenthalt. Der Patient kommt in die Klinik, wird anschließend operiert und geht noch am selben Tag wieder nach Hause. Die Vorteile liegen hierbei in der Frühmobilsieren des Patienten, der besseren Kalkulierbarkeit des zeitlichen Ablaufs, dem geringeren Risiko krankenhausbedingter Infektionen und eine bessere Auslastung des Spitalsbetriebs. Im Gegenteil, die Frühmobilisierung und die geringere Gefähr der Infektion (Spitalskeime) verküzt die Rekonvaleszenz merklich... weiter lesen.
Auszug aus dem möglichen ambul. OP-Katalog: - handchirurgische Eingriffe (Ganglion, Nagelplastik) - allgemeinchirurgische Eingriffe (Besenreiser entfernen lassen, Leisten- und Nabelbruch, Port-Anlage, Hautkrebs, Brusteingriffe) -sonstige Eingriffe (auch Dickdarmspiegelungen mit Polypen können ambulant durchgeführt werden)
Magen-Darmzentrum
 In Österreich erkranken jährlich über 5.000 Menschen an Dickdarmkrebs. Damit ist dieser eine der häufigsten Krebsformen. Beim Dickdarmkrebs ist die Vorsorge in der Lage, das Leiden nicht nur zu einem frühen und damit gut behandelbaren Zeitpunkt zu erkennen, sondern auch durch die prophylaktische Behandlung von gutartigen Vorstufen den Ausbruch der Krebserkrankung überhaupt zu verhindern.
In Österreich erkranken jährlich über 5.000 Menschen an Dickdarmkrebs. Damit ist dieser eine der häufigsten Krebsformen. Beim Dickdarmkrebs ist die Vorsorge in der Lage, das Leiden nicht nur zu einem frühen und damit gut behandelbaren Zeitpunkt zu erkennen, sondern auch durch die prophylaktische Behandlung von gutartigen Vorstufen den Ausbruch der Krebserkrankung überhaupt zu verhindern.
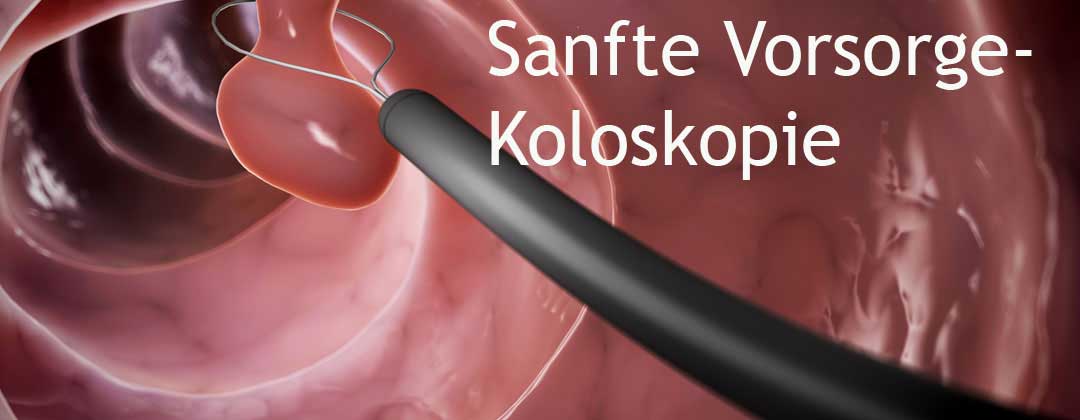
Seit Einführung der Vorsorgekoloskopie lassen sich in Österreich hunderte Darmkrebsneuerkrankungen und -todesfälle pro Jahr verhindern. Es könnten noch mehr sein – denn es macht einen Unterschied, ob die Untersuchung qualitätsgesichert durchgeführt wird oder nicht.
Venenbehandlung
 Krampfadern stören nicht nur kosmetisch. Sie verursachen auch Müdigkeit, Stauungsbeschwerden, Wadenkrämpfe, Hautveränderungen und wiederholt Venenentzündungen bis zur Entwicklung eines Geschwürs am Unterschenkel (venöses Ulcus). Im Anfangsstadium der Venenerkrankung kann versucht werden, die Venen zu veröden. Diese Verödung (Sklerosierung) ist jedoch nur bei Krampfadern unter 10mm empfohlen, bei voll ausgebildeten Krampfadern ist ein dauerhafter Erfolg kaum zu erwarten. Das gleiche gilt auch für Behandlungsmaßnahmen, wie das Tragen eines Gummistrumpfes und die Gabe von Medikamenten. Zur Operation können wir aber dann raten, wenn das tiefe Venensystem intakt ist. Dazu bedarf es eingehender Untersuchungen, z. B. der Doppler-Ultraschall, zur funktionellen Darstellung des Venensystems.
Krampfadern stören nicht nur kosmetisch. Sie verursachen auch Müdigkeit, Stauungsbeschwerden, Wadenkrämpfe, Hautveränderungen und wiederholt Venenentzündungen bis zur Entwicklung eines Geschwürs am Unterschenkel (venöses Ulcus). Im Anfangsstadium der Venenerkrankung kann versucht werden, die Venen zu veröden. Diese Verödung (Sklerosierung) ist jedoch nur bei Krampfadern unter 10mm empfohlen, bei voll ausgebildeten Krampfadern ist ein dauerhafter Erfolg kaum zu erwarten. Das gleiche gilt auch für Behandlungsmaßnahmen, wie das Tragen eines Gummistrumpfes und die Gabe von Medikamenten. Zur Operation können wir aber dann raten, wenn das tiefe Venensystem intakt ist. Dazu bedarf es eingehender Untersuchungen, z. B. der Doppler-Ultraschall, zur funktionellen Darstellung des Venensystems.
Doctify

Arzt-App
Mit dieser App bleiben Sie mit Ihrem Arzt in Verbindung. Herunterladen, Arzt-Code eingeben und schon können Sie einfach auch von unterwegs einen Termin vereinbaren.

Die Ordination hat kleine Kassen und Privat, Wahlarzt der GKK
Bringen Sie Folgendes mit:E-Card, Kranken- oder Zuweisungsschein, Entlassungsbriefe, Vorbefunde (Röntgenbilder, Blutlabor, usw.) mitbringen.

Wollen Sie einen Termin vereinbaren?
Vereinbaren Sie Ihren Beratungstermin mit uns schnell
und einfach online. Per Online-Formular oder während
unserer Ordinationszeiten auch im Online -Sekretariat.